Thermique : comment caractériser les échanges d’énergie sous forme thermique ?
Chaleur
La chaleur est un mode de transfert d’énergie (thermique) entre deux corps de températures différentes. La chaleur peut donc être une notion subjective :
Plongez votre main dans une eau à 5 °C puis sous un robinet d’eau à température ambiante et l’eau du robinet vous semblera chaude.

Plongez votre main dans une eau à 45 °C puis sous un robinet d’eau à température ambiante et l’eau du robinet vous semblera froide.
En fonction des circonstances une eau à température constante peut sembler chaude ou froide.
Température : mesure, unités et échelles
La température mesurée avec un thermomètre permet d’avoir une mesure plus objective et précise. La température mesure en fait l’agitation des atomes, ions, molécules qui constituent la matière.

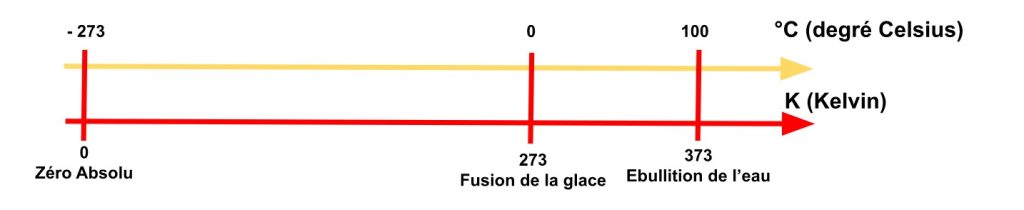
Le degré Celsius (° C) et le Kelvin (K) sont deux unités de températures. La température de 0 K ou zéro absolu (jamais atteinte dans l’univers) correspond à celle où la matière serait totalement immobile. Le zéro absolu correspond à une température de -273,15 ° C.
T (K) = θ (°C) + 273
θ (°C) = T (K) – 273
La mise en contact de deux corps de températures différentes entraîne un échange de chaleur jusqu’à un état d’équilibre thermique : les températures des 2 corps sont alors égales.
Changements d’état
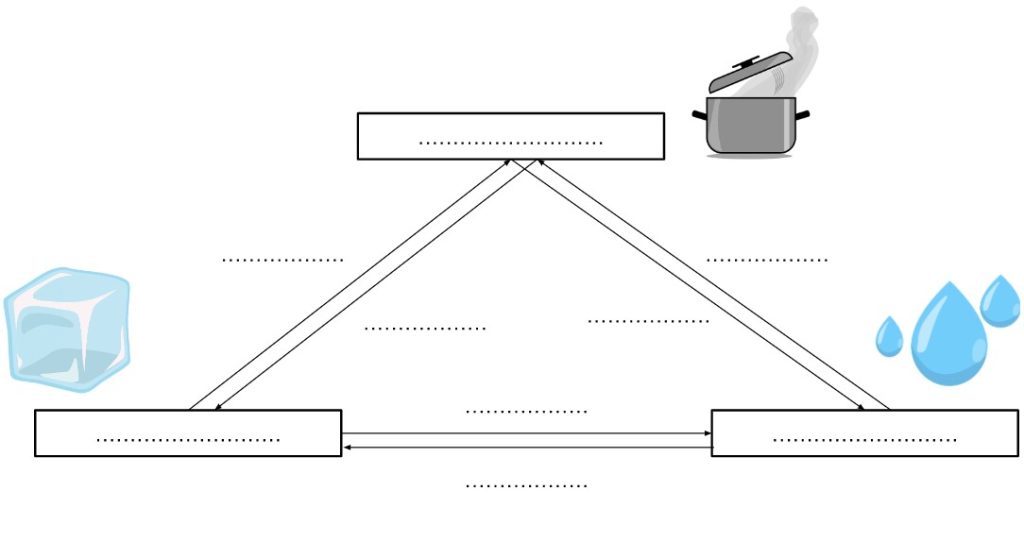
Un changement d’état peut-être provoqué en faisant varier :
– La température θ (°C), un apport d’énergie l’augmente, une perte la diminue.
– La pression p (Pa) (on peut faire bouillir de l’eau à 20 ° C sous vide)
Variation de température et changement d’état :
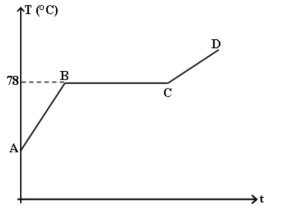
Le changement d’état d’un corps pur se fait à température constante, on observe un palier sur la courbe.
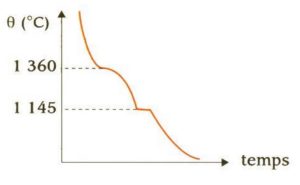
Solidification d’un acier (2 % de carbone, 98% de fer)
Le changement d’état d’un mélange s’accompagne d’un changement de température.
Exercices de thermique en CAP
Exercice 1 : changement d’état du bioéthanol

1.) Indiquer la température d’ébullition du bioéthanol.
…………………………………………………………………………………………………………….
2.) Indiquer la température de fusion du bioéthanol.
…………………………………………………………………………………………………………….
3.) En déduire l’état physique dans lequel se trouve ce produit s’il est stocké à 25 °C.
…………………………………………………………………………………………………………….
Exercice 2 : changement d’état du mercure
Le mercure est un métal dont la température de fusion est –39 °C et sa température d’ébullition est de 356 °C. Indiquer l’état du mercure à température ambiante de 20 °C et sous pression atmosphérique normale.
…………………………………………………………………………………………………………………………………………………………………………………………………………………………..
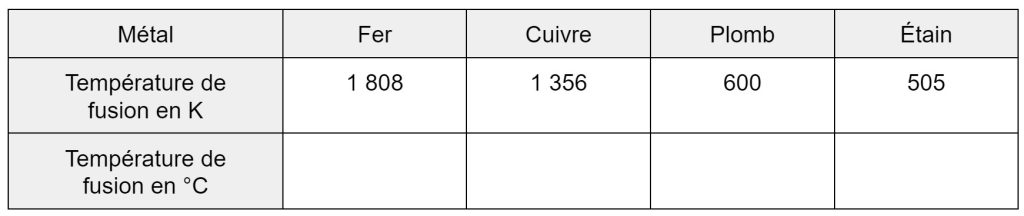
Exercice 3 : température de fusion des métaux.
Convertissez les températures de fusion de ces métaux en degré Celsius.
Exercice 3 : températures de changement d’état des corps purs et des mélanges.
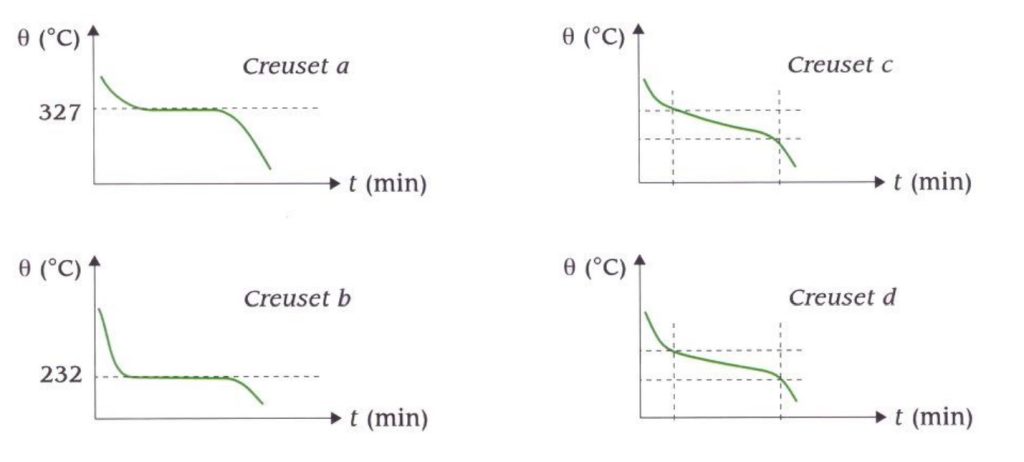
1.) Dans quel(s) creuset(s) trouve-t-on un alliage ? Justifier.
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….
2.) Dans quel(s) creuset(s) trouve-t-on un métal pur ? Justifier.
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….
3.) Quelle est la température de fusion de chaque métal pur ?
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….

3.) Quels sont les métaux purs considérés ?
……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………..
D’après S. GAUTIER
Compétences, capacités et connaissances issues du programme CAP Physique Chimie Education Nationale
Capacités
Mesurer des températures.
Utiliser un capteur de température.
Vérifier expérimentalement que deux corps en contact évoluent vers un état d’équilibre thermique.
Étudier expérimentalement l’évolution de la température d’un corps pur puis celle d’un mélange au cours de différents types de changements d’état.
Connaissances
Connaître les échelles de température : Celsius et Kelvin.
Connaître différents types de thermomètres.
Savoir que l’élévation (diminution) de température d’un corps nécessite un apport (une perte) d’énergie.
Savoir que la chaleur est un mode de transfert d’énergie (transfert thermique) entre deux corps de températures différentes.
Savoir qu’un changement d’état nécessite un transfert thermique sous forme de chaleur.

